Phê duyệt thuốc trị ung thư phổi trị giá hơn 4 tỷ đồng
2024-05-24T09:22:36+07:00 2024-05-24T09:22:36+07:00 https://songkhoe360.vn/canh-bao-59/phe-duyet-thuoc-tri-ung-thu-phoi-tri-gia-hon-4-ty-dong-3763.html /themes/default/images/no_image.gif
Sống khỏe 360 - Kênh thông tin tư vấn sức khỏe cộng đồng
https://songkhoe360.vn/uploads/final.png
22/05/2024 17:24 | Cảnh báo
 -
Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) vừa công bố việc cấp phép cho thuốc điều trị ung thư Imdelltra từ nhà sản xuất Amgen. Được biết, đây là một bước tiến quan trọng trong việc điều trị ung thư phổi tế bào nhỏ trong giai đoạn lan rộng tế bào ung thư sau hóa trị.
-
Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) vừa công bố việc cấp phép cho thuốc điều trị ung thư Imdelltra từ nhà sản xuất Amgen. Được biết, đây là một bước tiến quan trọng trong việc điều trị ung thư phổi tế bào nhỏ trong giai đoạn lan rộng tế bào ung thư sau hóa trị.
Theo kết quả thử nghiệm thuốc trên 99 người bệnh được công bố trên Tạp chí Y học New England hồi 2023, các nhà khoa học ghi nhận khối u trong cơ thể 40% bệnh nhân đã có sự teo nhỏ sau khi sử dụng thuốc Imdelltra. Điều đáng chú ý là thời gian sống trung bình của những người bệnh trong nghiên cứu là 14,3 tháng, so với tỷ lệ sống thông thường chỉ khoảng 5 tháng.
Một trong 99 người bệnh được thử nghiệm Imdelltra là bà Martha Warren, 65 tuổi, người Mỹ. Bà Warren đã phát hiện mình mắc ung thư phổi tế bào nhỏ và sau khi tìm hiểu, bà đã quyết định tham gia thử nghiệm lâm sàng của công ty Amgen.
Kết quả, sau khi được tiêm thuốc, tình trạng bệnh của bà bắt đầu có sự suy giảm đáng kể. Bà chia sẻ với New York Times rằng cảm thấy bình thường như trước khi mắc bệnh ung thư.
Tuy nhiên, việc sử dụng thuốc Imdelltra không phải là một quyết định dễ dàng do chi phí điều trị khá cao. Giá của thuốc tại Mỹ là 31.500 USD (hơn 800 triệu đồng) cho chu kỳ đầu tiên và 30.000 USD (hơn 763 triệu đồng) cho các chu kỳ tiếp theo. Ngoài ra, các bệnh nhân thử nghiệm sẽ phải chi trả tổng chi phí điều trị rơi vào khoảng 166.500 USD (hơn 4,2 tỷ đồng) trong thời gian trung bình hơn 5 tháng.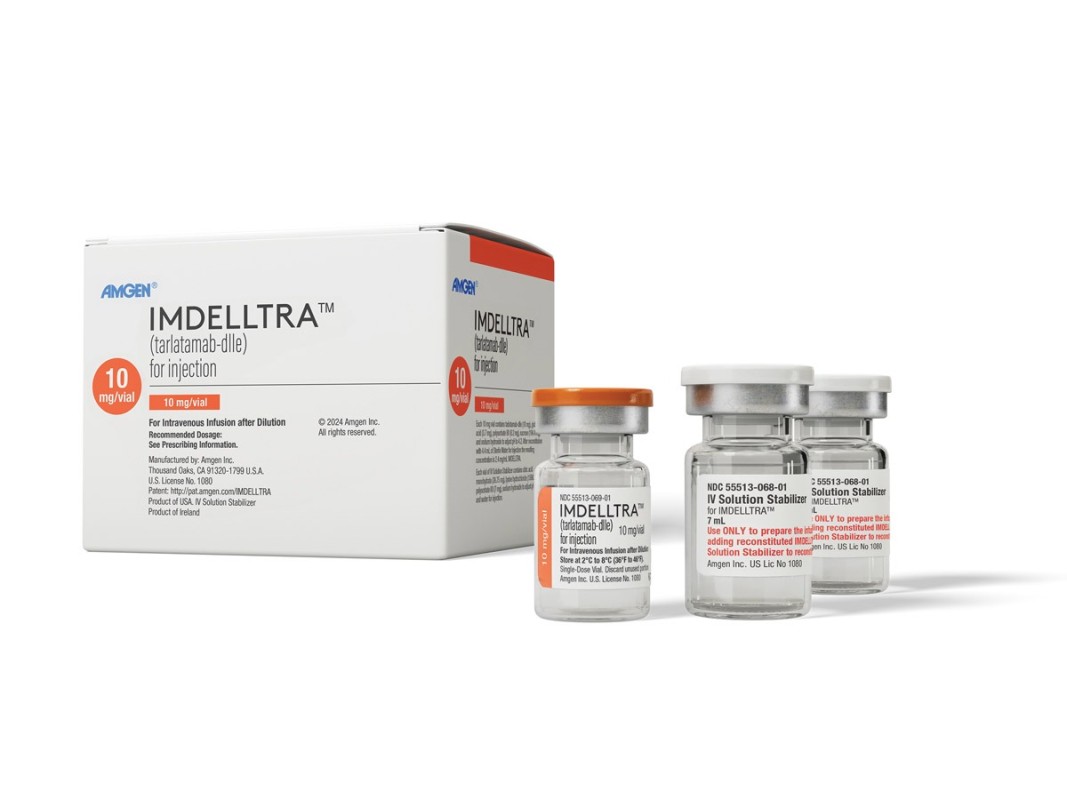 Đại diện của công ty Amgen cho biết rằng việc cấp phép cho thuốc Imdelltra là một bước tiến quan trọng trong việc cung cấp các phương pháp điều trị hiệu quả cho bệnh nhân mắc ung thư phổi tế bào nhỏ trong giai đoạn lan rộng tế bào ung thư sau hóa trị. Họ cũng cam kết tiếp tục nghiên cứu và phát triển các phương pháp điều trị mới để cung cấp hy vọng cho những người bệnh.
Đại diện của công ty Amgen cho biết rằng việc cấp phép cho thuốc Imdelltra là một bước tiến quan trọng trong việc cung cấp các phương pháp điều trị hiệu quả cho bệnh nhân mắc ung thư phổi tế bào nhỏ trong giai đoạn lan rộng tế bào ung thư sau hóa trị. Họ cũng cam kết tiếp tục nghiên cứu và phát triển các phương pháp điều trị mới để cung cấp hy vọng cho những người bệnh.
Trong khi đó, các chuyên gia y tế cũng đã đánh giá cao việc FDA cấp phép cho thuốc Imdelltra và hy vọng rằng việc này sẽ mở ra cơ hội mới trong điều trị ung thư phổi tế bào nhỏ. Tuy nhiên, họ cũng nhấn mạnh về tầm quan trọng của việc kiểm soát chi phí điều trị để đảm bảo rằng các phương pháp điều trị mới có thể tiếp cận được với nhiều người bệnh hơn.
Imdelltra là một loại thuốc trị liệu miễn dịch được sử dụng trong điều trị ung thư. Trong các thử nghiệm lâm sàng, tác dụng phụ thường gặp nhất của Imdelltra là gây ra hội chứng giải phóng cytokine (CRS). Hội chứng này xảy ra khi hệ thống miễn dịch của cơ thể phản ứng mạnh với thuốc trị liệu miễn dịch hoặc xuất hiện hiện tượng nhiễm trùng.
Hội chứng giải phóng cytokine là một phản ứng miễn dịch quá mức, gây ra sự tự giải phóng quá nhiều cytokine vào cơ thể. Người bị CRS có thể bị nhiễm độc thần kinh, ảnh hưởng đến tính mạng. Một số triệu chứng nhẹ hơn là mệt mỏi, sốt, rối loạn vị giác, chán ăn, đau cơ xương khớp, táo bón, thiếu máu và buồn nôn.
Để điều trị CRS, các biện pháp như sử dụng corticoid và thuốc kháng histamine có thể được áp dụng để kiểm soát phản ứng viêm và giảm triệu chứng.
FDA đánh giá Imdelltra theo khuôn khổ của Dự án Orbis, một sáng kiến của Trung tâm Ung thư trực thuộc cơ quan này. Dự án Orbis cung cấp khuôn khổ để đệ trình và xem xét đồng thời các loại thuốc điều trị ung thư. Để thực hiện đánh giá, FDA hợp tác với Cơ quan quản lý y tế Brazil (ANVISA), Bộ y tế Canada (HC), Bộ Y tế Israel (IMoH) và Cơ quan quản lý thuốc và sản phẩm chăm sóc sức khỏe của Vương quốc Anh (MHRA).
Để thực hiện đánh giá, FDA hợp tác với Cơ quan quản lý y tế Brazil (ANVISA), Bộ y tế Canada (HC), Bộ Y tế Israel (IMoH) và Cơ quan quản lý thuốc và sản phẩm chăm sóc sức khỏe của Vương quốc Anh (MHRA).
Theo ông Jay Bradner, Giám đốc Khoa học của Công ty dược Amgen, hàng năm có khoảng 35.000 người Mỹ được chẩn đoán mắc ung thư phổi. Đây là “một trong những bệnh ung thư phát triển nhanh và dễ ảnh hưởng xấu tới sức khỏe nhất”.
Công ty vẫn cần hoàn thành các thử nghiệm lớn hơn đối với thuốc điều trị ung thư phổi tế bào nhỏ giai đoạn muốn để sớm được FDA chấp thuận. Ngoài ra, công ty này cũng đang thử nghiệm thuốc điều trị ung thư phổi tế bào nhỏ giai đoạn đầu.
Kết luận
Imdelltra là một trong những lựa chọn điều trị ung thư tiên tiến, tuy nhiên, việc quản lý tác dụng phụ và đảm bảo an toàn cho bệnh nhân vẫn là một thách thức lớn đối với cộng đồng y học và ngành công nghiệp dược phẩm. Việc hợp tác quốc tế trong việc đánh giá và kiểm soát chất lượng sản phẩm là cần thiết để đảm bảo hiệu quả và an toàn trong điều trị ung thư.
Một trong 99 người bệnh được thử nghiệm Imdelltra là bà Martha Warren, 65 tuổi, người Mỹ. Bà Warren đã phát hiện mình mắc ung thư phổi tế bào nhỏ và sau khi tìm hiểu, bà đã quyết định tham gia thử nghiệm lâm sàng của công ty Amgen.
Kết quả, sau khi được tiêm thuốc, tình trạng bệnh của bà bắt đầu có sự suy giảm đáng kể. Bà chia sẻ với New York Times rằng cảm thấy bình thường như trước khi mắc bệnh ung thư.
Tuy nhiên, việc sử dụng thuốc Imdelltra không phải là một quyết định dễ dàng do chi phí điều trị khá cao. Giá của thuốc tại Mỹ là 31.500 USD (hơn 800 triệu đồng) cho chu kỳ đầu tiên và 30.000 USD (hơn 763 triệu đồng) cho các chu kỳ tiếp theo. Ngoài ra, các bệnh nhân thử nghiệm sẽ phải chi trả tổng chi phí điều trị rơi vào khoảng 166.500 USD (hơn 4,2 tỷ đồng) trong thời gian trung bình hơn 5 tháng.

Trong khi đó, các chuyên gia y tế cũng đã đánh giá cao việc FDA cấp phép cho thuốc Imdelltra và hy vọng rằng việc này sẽ mở ra cơ hội mới trong điều trị ung thư phổi tế bào nhỏ. Tuy nhiên, họ cũng nhấn mạnh về tầm quan trọng của việc kiểm soát chi phí điều trị để đảm bảo rằng các phương pháp điều trị mới có thể tiếp cận được với nhiều người bệnh hơn.
Imdelltra là một loại thuốc trị liệu miễn dịch được sử dụng trong điều trị ung thư. Trong các thử nghiệm lâm sàng, tác dụng phụ thường gặp nhất của Imdelltra là gây ra hội chứng giải phóng cytokine (CRS). Hội chứng này xảy ra khi hệ thống miễn dịch của cơ thể phản ứng mạnh với thuốc trị liệu miễn dịch hoặc xuất hiện hiện tượng nhiễm trùng.
Hội chứng giải phóng cytokine là một phản ứng miễn dịch quá mức, gây ra sự tự giải phóng quá nhiều cytokine vào cơ thể. Người bị CRS có thể bị nhiễm độc thần kinh, ảnh hưởng đến tính mạng. Một số triệu chứng nhẹ hơn là mệt mỏi, sốt, rối loạn vị giác, chán ăn, đau cơ xương khớp, táo bón, thiếu máu và buồn nôn.
Để điều trị CRS, các biện pháp như sử dụng corticoid và thuốc kháng histamine có thể được áp dụng để kiểm soát phản ứng viêm và giảm triệu chứng.
FDA đánh giá Imdelltra theo khuôn khổ của Dự án Orbis, một sáng kiến của Trung tâm Ung thư trực thuộc cơ quan này. Dự án Orbis cung cấp khuôn khổ để đệ trình và xem xét đồng thời các loại thuốc điều trị ung thư.

Theo ông Jay Bradner, Giám đốc Khoa học của Công ty dược Amgen, hàng năm có khoảng 35.000 người Mỹ được chẩn đoán mắc ung thư phổi. Đây là “một trong những bệnh ung thư phát triển nhanh và dễ ảnh hưởng xấu tới sức khỏe nhất”.
Công ty vẫn cần hoàn thành các thử nghiệm lớn hơn đối với thuốc điều trị ung thư phổi tế bào nhỏ giai đoạn muốn để sớm được FDA chấp thuận. Ngoài ra, công ty này cũng đang thử nghiệm thuốc điều trị ung thư phổi tế bào nhỏ giai đoạn đầu.
Kết luận
Imdelltra là một trong những lựa chọn điều trị ung thư tiên tiến, tuy nhiên, việc quản lý tác dụng phụ và đảm bảo an toàn cho bệnh nhân vẫn là một thách thức lớn đối với cộng đồng y học và ngành công nghiệp dược phẩm. Việc hợp tác quốc tế trong việc đánh giá và kiểm soát chất lượng sản phẩm là cần thiết để đảm bảo hiệu quả và an toàn trong điều trị ung thư.
Ý kiến bạn đọc
Tổng hợp các bài viết
Cập nhật liên tục, nhanh chóng






















